[초점]'카티라이프' 이후‥세포치료제, 5년간 국내 허가 없어
첨단바이오약품으로 2002년부터 수입산 아닌 제조 품목 13개 식약처 허가
'첨생법' 시행 뒤 줄기세포藥 등 재허가에도 다수 제품 투여 어려워 지적돼
[초점]'카티라이프' 이후‥세포치료제, 5년간 국내 허가 없어첨단바이오약품으로 2002년부터 수입산 아닌 제조 품목 13개 식약처 허가
|
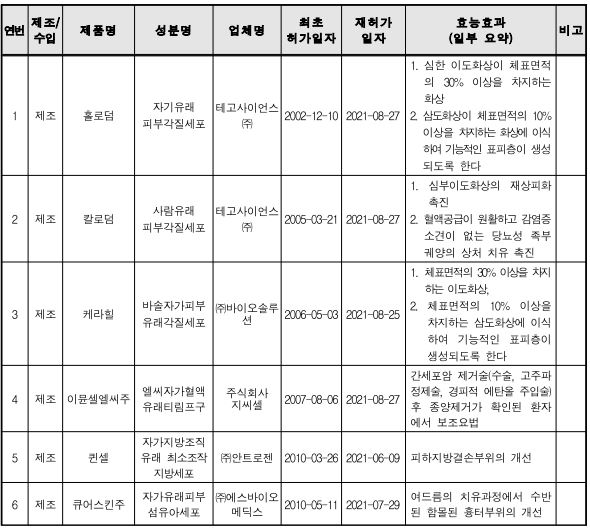 |
 세포치료제 허가 현황 <자료 : 식약처> |
세포치료제는 약 4년 전 '첨단재생바이오법(첨생법)'이 시행된 후 3년 전 이 품목들이 모두 재허가를 받기도 했다.
그러나 재허가를 받았어도 다수 세포치료제는 건강보험 문제 등으로 환자들에게 쉽게 투여될 수 없다는 지적이 제기되고 있다.
바이오의약품협회에 따르면 국내 세포·유전자치료제 시장 규모는 1,155억(2022년)으로 전년 대비 약 38% 급증했고, 생산 실적은 약 840억(2022년)으로 집계됐으며, 이 중 생산 실적이 큰 제품은 이뮨셀-LC, 카티스템, 칼로덤, '케라힐'(바이오솔루션), '케라힐-알로'(바이오솔루션), 뉴로나타-R, 카티라이프, 홀로덤, 하티셀그램-AMI, 큐피스템 등의 순으로 나타났다.
 |




















